-
+86-510-81810835
- Hzw@sunkeycn.com
![F-значение и валидация процесса реторт-пакетов [2026] | Sunkey - ООО Цзянсу Шэнькай Упаковочные Высокие Технологии](https://www.sunkeypackaging.ru/wp-content/themes/global/static/images/closeBtn.png)
+86-510-81810835
![F-значение и валидация процесса реторт-пакетов [2026] | Sunkey - ООО Цзянсу Шэнькай Упаковочные Высокие Технологии](https://www.sunkeypackaging.ru/wp-content/themes/global/static/images/closeBtn.png)
2026-03-04
| КРАТКИЙ ОТВЕТ: Что необходимо для валидации процесса реторт-пакетов перед коммерческим производством?
• F₀ (эквивалентные минуты при 121°C) должно достигнуть значения планового процесса — минимум F₀ = 3,0 мин для низкокислотных продуктов согласно 21 CFR Part 113. • Исследование распределения тепла (HDS) и исследование теплопроникновения (HPS) — два отдельных обязательных этапа, ни один из которых нельзя заменить другим. • Холодная точка (место наиболее медленного нагрева в продукте) должна быть подтверждена в HDS, прежде чем термопары HPS смогут быть правильно размещены. • Квалифицированный Технологический орган (Process Authority) должен разработать и подписать документ планового процесса до начала коммерческих продаж. • Полный срок валидации: минимум 14–22 недели. Инкубационный тест продолжительностью 10 дней невозможно сократить никакими средствами. • Продажа реторт-продуктов в США без зарегистрированного планового процесса является федеральным правонарушением по 21 CFR Part 113. |
1.Почему валидацию процесса нельзя пропустить
2.F-значение: единица измерения термической летальности
3.Исследование распределения тепла (HDS): шаг 1 — квалификация реторт-устройства
4.Исследование теплопроникновения (HPS): шаг 2 — измерение летальности в холодной точке
5.Расчёт F₀: от данных время-температура до числа соответствия нормам
6.Технологический орган (Process Authority): кто это и что он должен подписать
7.FDA 21 CFR Part 113: требования к регистрации для рынка США
8.Полный временной план: 14–22 недели, которые невозможно сократить
9.Целевые значения F₀ по типу применения и продукта
10.Шесть ошибок валидации, задерживающих запуск на месяцы
11.Часто задаваемые вопросы
Валидация процесса для реторт-пакетов — это не бюрократическая формальность. Это научное доказательство того, что ваш конкретный продукт, в вашей конкретной структуре пакета, обработанный в вашем конкретном реторт-устройстве, каждый раз достигает коммерческой стерильности. Без неё у вас есть гипотеза, а не безопасный продукт.
Последствием пропуска или сокращения валидации является не регуляторное неудобство. Для низкокислотных пищевых продуктов — а к ним относятся практически все продукты из мяса, корма для животных, морепродуктов и готовые блюда — недостаточная стерилизация позволяет выжить Clostridium botulinum и производить ботулотоксин внутри упаковки. Это один из наиболее мощных известных биологических токсинов: летален в нанограммовых количествах, бесцветен, не имеет запаха и не определяется без лабораторного анализа.
| Важно: Согласно 21 CFR Part 113 (FDA), ни один низкокислотный реторт-продукт не может коммерчески распространяться в США без планового процесса, разработанного квалифицированным Process Authority и зарегистрированного в FDA. Нарушение является федеральным правонарушением и влечёт обязательный отзыв продукции, закрытие завода и возможное уголовное преследование. |
Каждый этап описанной в этой статье системы валидации существует благодаря задокументированным историческим авариям: вспышкам ботулизма, массовым отзывам и смертельным случаям, связанным с недостаточной термической обработкой. Временной план в 14–22 недели не произвольный — каждый этап генерирует конкретные данные, которые невозможно получить иным способом или за более короткое время.
| Совет: Если вы переходите с консервных банок на реторт-пакеты и уже имеете валидированный консервированный продукт, существующие данные валидации не переносятся. Пакеты нагреваются иначе, чем банки — расположение холодной точки, скорость теплопроникновения и профиль накопления F₀ отличаются и должны быть заново установлены для формата пакета. |
F-значение (конкретно F₀, произносится «F-нуль») — это количественная мера способности термического процесса уничтожать микроорганизмы. Оно выражается в эквивалентных минутах обработки при 121°C (250°F) — стандартной референсной температуре для стерилизации низкокислотных пищевых продуктов.
Для понимания F₀ необходимо знать два связанных понятия: D-значение и z-значение. D-значение — это время при данной температуре, необходимое для снижения популяции бактерий на 90% (один log-цикл). Для спор Clostridium botulinum в продукте с нейтральным pH значение D₁₂₁ составляет приблизительно 0,21 минуты. z-значение описывает, как D-значение изменяется с температурой — для C. botulinum z-значение равно 10°C, то есть при каждом повышении температуры на 10°C D-значение уменьшается в десять раз (уничтожение происходит в 10 раз быстрее).
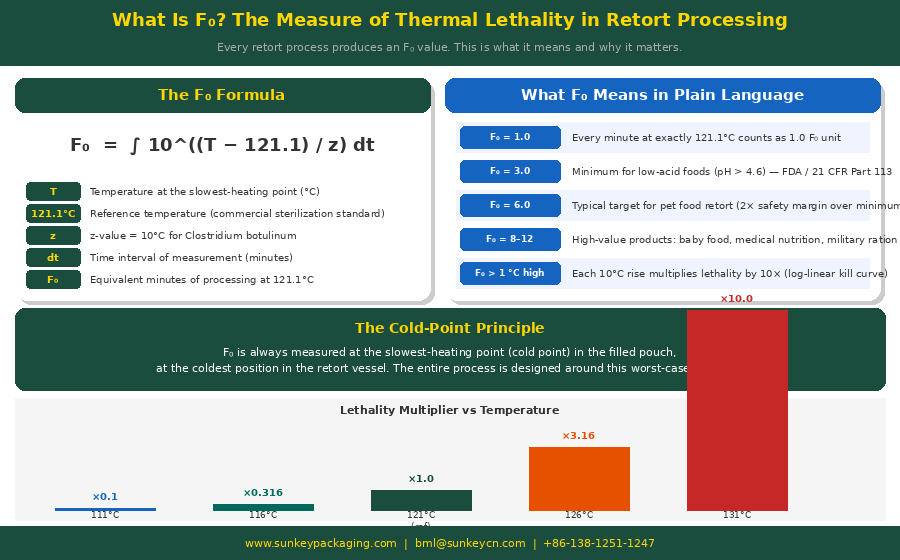
Эти зависимости определяют летальную скорость (L) — безразмерное число, выражающее эффективность температуры в данный момент времени по отношению к референсной 121°C: L = 10^((T − 121) / 10). При 121°C: L = 1,0. При 131°C: L = 10,0 — в десять раз более летально за минуту. При 111°C: L = 0,1 — в десять раз менее летально. F₀ — это интеграл L по всему времени обработки: F₀ = ∫L dt, суммированный с интервалами (обычно каждые 30 секунд) на протяжении фаз разогрева, выдержки и охлаждения ретортного цикла.
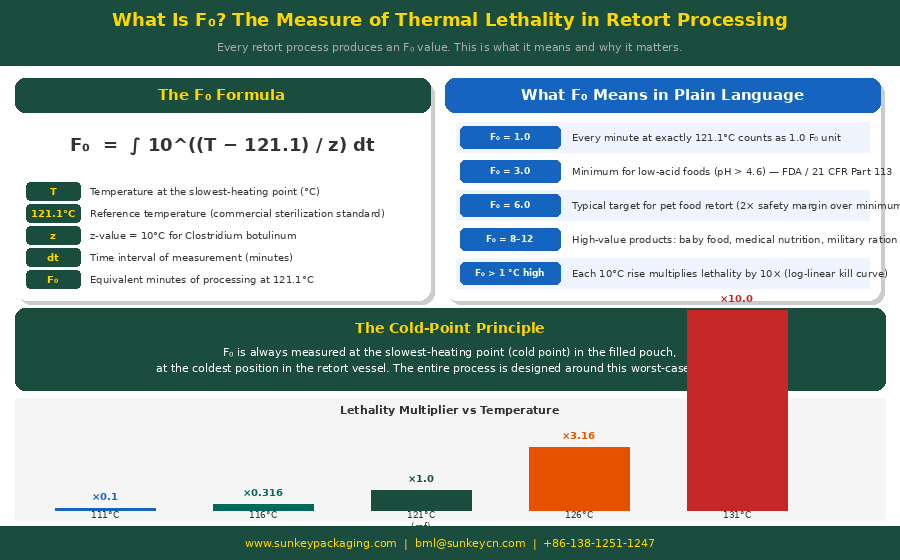
Регуляторный минимум F₀ для низкокислотных пищевых продуктов согласно 21 CFR Part 113 составляет 3,0 минуты — это соответствует снижению на 12 порядков (12D) спор C. botulinum, что является международным принятым стандартом безопасности пищевых продуктов. На практике большинство коммерческих продуктов проектируется со значительно более высокими значениями F₀ (6–15 минут) для обеспечения запаса безопасности.
| Примечание: F₀ = 3,0 минуты не означает обработку в течение 3 минут. Это означает, что накопленная летальность, проинтегрированная по всей кривой время-температура — включая разогрев и охлаждение — должна быть эквивалентна как минимум 3 минутам воздействия при 121°C. Выдержка 30 минут при 121°C даёт F₀ ≈ 31 минуту, что значительно превышает минимум и является типичным для многих пищевых продуктов. |
Исследование распределения тепла отвечает на один вопрос: равномерно ли распределяется пар по всему реторт-устройству в процессе обработки? Если нет — если определённые зоны внутри устройства нагреваются медленнее других — то пакеты, обрабатываемые в этих холодных зонах, могут не получить требуемого F₀, даже если референсная термопара реторта показывает правильную температуру.
HDS проводится без продукта в устройстве — оно характеризует само устройство, а не продукт. Несколько термопар (минимум 9, обычно 12–16 на устройство согласно руководству NFPA Bulletin 26) размещаются в критических точках по всему объёму устройства: спереди, сзади, вверху, внизу, по центру и вблизи входного патрубка пара и отвода конденсата. Затем устройство эксплуатируется в полных циклах при целевой температуре обработки.

Критерий приёмки для HDS: все позиции термопар должны достичь целевой температуры стерилизации в течение запланированного времени разогрева, а разброс температур по всем позициям не должен превышать 0,5°C после начала фазы выдержки. Это подтверждает, что каждый пакет, загруженный в любую позицию устройства, получит эквивалентное тепловое воздействие.
| Что устанавливает HDS
Идентификация холодной зоны: наиболее медленно нагревающееся место в устройстве. Именно здесь должна быть размещена термопара HPS. Подтверждение времени разогрева: время от начала процесса до момента достижения целевой температуры во всех точках устройства. Проверка схемы вентилирования: последовательность удаления воздуха перед заполнением паром — критически важна для равномерного распределения. Квалификация устройства: официальная документация, подтверждающая, что данное конкретное устройство в данной конфигурации квалифицировано для использования в плановых процессах. База для оценки отклонений процесса: при возникновении температурного отклонения во время производства данные HDS используются для расчёта фактически доставленного F₀. |
| Важно: HDS должна проводиться заново при любом изменении, перемещении или значительном ремонте реторт-устройства. Также необходима повторная HDS при существенном изменении схемы загрузки — устройство, квалифицированное для конкретного способа укладки, не является автоматически квалифицированным для другой ориентации пакетов или плотности загрузки. |
| Совет: HDS требует минимум 3 последовательных воспроизводимых запуска при целевой температуре. Если какой-либо запуск показывает разброс более 0,5°C или зону, не достигающую температуры в пределах времени разогрева, необходимо исследовать процедуру вентилирования и подачу пара перед повторным проведением исследования. |
Если HDS характеризует устройство, то HPS характеризует продукт. Исследование теплопроникновения отвечает на другой, более критичный вопрос: как быстро тепло проникает в наиболее холодную точку внутри наполненного, запечатанного пакета — и сколько F₀ накапливается в этой точке за полный цикл обработки?
Холодная точка в продукте реторт-пакета — это место, которое нагревается наиболее медленно. Для однородных жидких или полужидких продуктов (бульоны, паштеты, влажный корм для животных) теплопередача происходит преимущественно путём конвекции, и холодная точка обычно находится в геометрическом центре пакета — в точке, наиболее удалённой от всех нагреваемых поверхностей. Для твёрдых или содержащих частицы продуктов с ограниченной конвекцией холодная точка может находиться в центре наиболее крупного твёрдого куска и должна быть определена эмпирически.
HPS проводится с производственно-репрезентативными наполненными пакетами — та же рецептура, тот же вес наполнения, то же пространство над продуктом, та же структура пакета, что и в коммерческом продукте. Откалиброванные термопары вводятся в пакет через герметизированный вводной элемент и размещаются в холодной точке, подтверждённой HDS. Пакеты загружаются в реторт-устройство в позицию холодной зоны, подтверждённую HDS, и обрабатываются в полных циклах.
| Примечание: Вводной элемент термопары не должен нарушать герметичный шов пакета. Валидированные фитинги для ввода ТС, специально разработанные для HPS реторт-пакетов, доступны у поставщиков, включая Ellab и Mesa Labs. Никогда не используйте самодельные методы ввода, которые могут повлиять на теплопередачу или целостность шва. | |
| Минимальные требования к HPS согласно 21 CFR Part 113 и NFPA Bulletin 26
Минимум 3 последовательных производственных запуска: каждый запуск должен достичь целевого F₀. Одного успешного запуска недостаточно. ТС в подтверждённой холодной точке: термопара размещается в позиции холодной зоны по HDS, в холодной точке продукта по HPS. Производственный вес наполнения и пространство над продуктом: HPS должна воспроизводить условия промышленного производства. Интервал регистрации данных: максимум 0,5 минуты (30 секунд). Рекомендуется более частая регистрация (10-секундные интервалы). Калибровка ТС до и после исследования: каждая термопара должна быть откалиброван с точностью ±0,1°C. Дрейф более ±0,2°C требует повторного исследования. Проверка Process Authority: все первичные данные, расчёты и заключения должны быть проверены и подписаны Process Authority до установления планового процесса. |
|
Расчёт F₀ прост при наличии данных время-температура из HPS. Расчёт выполняется в три шага применительно к данным температуры холодной точки, собранным во время HPS.
Шаг 1: для каждой точки во времени рассчитать летальную скорость (L) по формуле L = 10^((T − 121) / 10), где T — температура холодной точки в градусах Цельсия в данный момент времени. При температурах ниже примерно 90°C значение L настолько мало, что им пренебрегают. Шаг 2: умножить каждое значение L на временной интервал (Δt, обычно 0,5 минуты), чтобы получить вклад летальности каждого интервала. Шаг 3: суммировать все вклады летальности от нулевого момента времени (закрытие двери реторта) до конца фазы охлаждения. Эта сумма и является значением F₀.
Для типичного цикла обработки при 121°C с 30-минутной выдержкой разбивка F₀ приблизительно такова: фаза разогрева вносит около 0,5–2,0 минут F₀; фаза выдержки при 121°C вносит F₀, равное времени выдержки в минутах; фаза охлаждения вносит около 0,5–1,5 минут F₀. Общее F₀ для 30-минутного цикла при 121°C обычно составляет 32–34 минуты — значительно выше минимального требования для большинства низкокислотных пищевых продуктов.
| Совет: При процессе реторт 135°C летальная скорость при температуре выдержки составляет L = 10^((135−121)/10) = 25,1 — это означает, что каждая минута при 135°C эквивалентна 25 минутам при 121°C по термической летальности. Реторт-пакет, обработанный при 135°C всего 4 минуты, может накопить F₀ > 100 минут — именно поэтому высокотемпературные процессы могут использовать значительно более короткое время выдержки. | ||
| Параметр | Процесс 121°C | Процесс 135°C |
| Температура выдержки | 121°C (250°F) | 135°C (275°F) |
| Летальная скорость (L) при выдержке | 1,0 (референс) | 25,1 |
| Типичное время выдержки (корм для животных) | 20–45 минут | 3–8 минут |
| Типичное достигнутое F₀ | 25–50 минут | 80–200+ минут |
| Минимум F₀ (низкокислотные) | ≥ 3,0 мин | ≥ 3,0 мин |
| Требуемый внутренний слой | RCPP или стандартный CPP | Только RCPP (ретортный) |
| Требуемый ламинат | PET/Al/CPP или PET/Al/RCPP | PET/Al/PA/RCPP или PET/Al/RCPP |
Process Authority (технологический орган) — это лицо или организация, обладающие научной компетентностью, опытом и квалификацией для оценки и разработки плановых процессов для термически обработанных пищевых продуктов. Согласно 21 CFR Part 113, ни один плановый процесс для низкокислотного пищевого продукта не может коммерчески использоваться, если он не был разработан компетентным технологическим органом.
Понятие «компетентный технологический орган» определяется FDA как лицо, обладающее экспертными знаниями, полученными в результате соответствующей подготовки и опыта в области научных принципов и методов установления термических процессов для низкокислотных пищевых продуктов. На практике это означает лицо или организацию с формальной подготовкой в области пищевых наук, микробиологии и теплопередачи, как правило подтверждённой квалификацией IFT, NFPA или аккредитованной университетской программой по пищевым наукам.

| Что должен сделать Process Authority
1. Проверить и подтвердить все первичные данные HDS и HPS на техническую адекватность и точность. 2. Выполнить или верифицировать расчёт F₀ и подтвердить, что плановый процесс обеспечивает требуемую летальность в холодной точке. 3. Разработать документ планового процесса с указанием: максимального веса наполнения, минимальной начальной температуры, температуры реторта, времени обработки (разогрев + выдержка), протокола охлаждения, типа и размеров контейнера. 4. Подписать документ планового процесса — эта подпись означает профессиональную сертификацию того, что процесс обеспечивает коммерческую стерильность. 5. Рассматривать любые отклонения процесса, возникающие в ходе производства, и определять, является ли продукция безопасной для распространения. 6. Для рынка США: подготовить или проверить документацию для регистрации процесса в FDA. |
| Важно: Process Authority не может просто подписать ваши внутренние расчёты. Ему необходим доступ к первичным файлам данных HDS и HPS, записям о калибровке, документации о размещении термопар и рабочим записям реторта. Если Process Authority готов выдать документ планового процесса без проверки этих данных, это следует считать серьёзным тревожным сигналом. |
В США термически обработанные низкокислотные пищевые продукты в герметично закрытых контейнерах — в том числе прямо указанные реторт-пакеты — регулируются 21 CFR Part 113, нормативом по низкокислотным консервированным продуктам (LACF). Этот норматив действует с 1979 года и применяется к любой компании, производящей такие продукты для продажи в США, независимо от места производства.
Основное требование к регистрации содержится в 21 CFR Part 113.40: плановый процесс для каждой комбинации продукт/контейнер/реторт должен быть зарегистрирован в FDA до начала коммерческого распространения. Регистрация подаётся через систему регистрации процессов FDA (PFS) с использованием формы FDA 2541a (для непрерывных ретортных систем) или FDA 2541d (для периодических ретортных систем).
| Требование | Содержание | Ссылка | |
| Регистрация процесса | Обязательна до первой коммерческой продажи в США | 21 CFR Part 113.40 | |
| Основание планового процесса | Должен быть разработан компетентным Process Authority | 21 CFR Part 113.83 | |
| Форма регистрации | FDA 2541a (непрерывный) или FDA 2541d (периодический реторт) | Система регистрации LACF FDA | |
| Регистрация предприятия | Все предприятия LACF должны быть зарегистрированы в FDA | 21 CFR Part 113.35 | |
| Хранение записей | Все записи процесса: минимум 3 года | 21 CFR Part 113.100 | |
| Отклонения процесса | Должны оцениваться Process Authority до распространения | 21 CFR Part 113.89 | |
| Инкубационный тест | Обязателен для проверки коммерческой стерильности | 21 CFR Part 113.87 | |
| Проверка pH | Низкокислотный = pH > 4,6; должен быть задокументирован | 21 CFR Part 113.40(a) | |
| Примечание: Для выхода на рынок ЕС эквивалентная нормативная база — Регламент ЕС 852/2004 (гигиена пищевых продуктов) и Регламент ЕС 853/2004 (специальные правила гигиены для продуктов животного происхождения). В ЕС нет прямого аналога системы регистрации процессов LACF США, однако те же научные стандарты валидации (расчёт F₀, проверка Process Authority) применяются и ожидаются европейскими органами по безопасности пищевых продуктов. Российские стандарты серии ГОСТ Р также требуют документации о валидации процесса. | |||
| Совет: Китайские производители, экспортирующие реторт-пакеты в США, должны убедиться, что их американский импортёр зарегистрировал плановый процесс в FDA до первой поставки. Это часто упускаемый шаг в коммерческом плане. Обработка регистрации в FDA обычно занимает 2–4 недели, и до её завершения продукт не может быть законно продан в США. | |||
Понимание временного плана валидации процесса критически важно для любого производителя, планирующего запуск реторт-продукта или переход с банок на пакеты. Диапазон 14–22 недели — это не консервативный запас, а минимальная длительность каждого этапа, определяемая либо биологической реальностью (инкубация), либо объёмом данных, которые необходимо собрать и проверить.
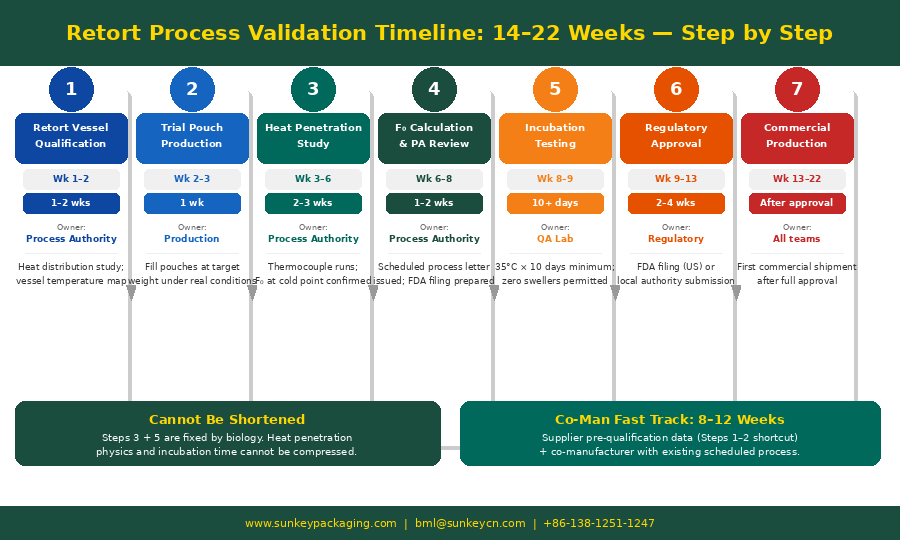
| Этап | Мероприятия | Минимальная длительность | Можно ли сократить? |
| 1. Исследование распределения тепла | Размещение ТС, 3+ запуска реторта, калибровка, анализ данных | 1–2 недели | Только при использовании предварительно квалифицированных данных реторта от Sunkey или коупакера |
| 2. Исследование теплопроникновения | Ввод ТС, 3+ производственных запуска при рабочем весе наполнения, калибровка | 2–3 недели | Минимум 3 запуска нельзя сократить; запуски могут следовать подряд |
| 3. Анализ данных + Process Authority | Расчёт F₀, проверка PA, документ планового процесса | 1–2 недели | Зависит от доступности PA — бронируйте заранее |
| 4. Инкубационный тест | 24+ пакета при 35°C в течение ровно 10 дней | 2 недели (фиксировано) | Нет — биологический тест, нельзя ускорить ни при каких обстоятельствах |
| 5. Регистрация в FDA (рынок США) | Подготовка форм 2541a/d, подача, рассмотрение FDA | 2–4 недели | Время рассмотрения устанавливается FDA; возможности ускорения ограничены |
| ИТОГО | 14–22 недели минимум | Только этап 1 можно сократить с предварительно квалифицированными данными устройства | |
| Важно: Не начинайте коммерческое распространение, даже на тестовых рынках или пилотным клиентам, до завершения этапа 5 (для продукта, поставляемого в США) или этапа 4 без нарушений (для всех рынков). Любой продукт, произведённый до прохождения инкубации, должен быть помещён в карантин. При обнаружении нарушений инкубации вся партия должна быть уничтожена, а причина расследована до повторного проведения исследования. | |||
Минимум FDA в 3,0 минуты — это порог, а не цель. Коммерческие плановые процессы разрабатываются со значительным запасом превышения этого минимума, а подходящее целевое F₀ зависит от типа продукта, pH, активности воды и требуемого консерватизма процесса.
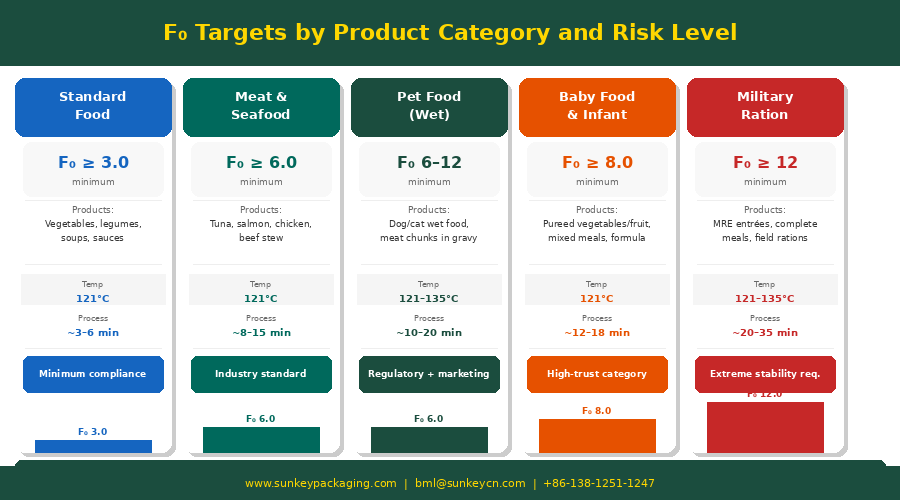
| Применение | Типичная цель F₀ | Обоснование / примечания |
| Влажный корм для животных (кусочки в соусе) | F₀ = 6–10 мин | Стандартный коммерческий запас безопасности; pH обычно 6,0–7,0 |
| Влажный корм (паштет/рулет, полностью мясной) | F₀ = 8–15 мин | Более высокое F₀ для плотного продукта с ограниченной конвекцией |
| Готовые блюда (рагу, карри) | F₀ = 8–12 мин | Консервативный подход для прямого потребления человеком |
| Детское питание (пюре, мясо/овощи) | F₀ = 12–18 мин | Максимальный запас безопасности; уязвимая группа потребителей |
| Морепродукты (тунец, лосось, моллюски) | F₀ = 6–10 мин | Зависит от pH; некоторые виды имеют повышенный риск термофилов |
| Военный паёк / продукты длительного хранения | F₀ = 15–25 мин | Увеличенный срок хранения (5–7 лет) требует более высокого запаса |
| Подкисленные продукты (pH < 4,6) | Не требуется | Ниже pH 4,6 C. botulinum не может размножаться — применяется иная нормативная база |
| Примечание: Эти целевые значения F₀ представляют собой отраслевые стандарты и принятую практику — они не являются универсально обязательными для FDA при этих конкретных значениях. Ваш Process Authority устанавливает плановое F₀ для вашего конкретного продукта на основе рецептуры, pH продукта, максимального веса наполнения и геометрии контейнера. Не применяйте целевое F₀ другого производителя к своему продукту без независимой валидации. | ||
Каждая из следующих ошибок добавляет 4–12 недель к временному плану валидации, поскольку требует повторного прохождения соответствующего этапа с нуля. Все шесть ошибок можно предотвратить при надлежащем планировании.

Наиболее значимая ошибка: проведение HPS с термопарой, размещённой в предполагаемой, а не подтверждённой HDS холодной точке. Если ТС не находится в истинной холодной точке, измеренное F₀ в ходе HPS будет выше фактического. Плановый процесс будет основан на завышенных данных летальности. Это одновременно ошибка безопасности пищевых продуктов и нарушение регуляторных требований. Профилактика: всегда завершайте HDS перед HPS.
Термопара с дрейфом более ±0,2°C между предварительной и последующей калибровкой обесценивает данные, собранные в ходе этого исследования. Учитывая зависимость L = 10^((T−121)/10), ошибка в 1°C при 121°C вызывает погрешность F₀ на 8%. Профилактика: калибруйте все ТС в течение 24 часов до начала исследования; выполняйте повторную калибровку сразу после завершения последнего запуска.
HPS должна проводиться при максимальном коммерческом весе наполнения продукта. Более тяжёлое наполнение создаёт бо́льшую тепловую массу, замедляет теплопроникновение и снижает F₀ в холодной точке. Профилактика: указывайте допуск веса наполнения в протоколе HPS; взвешивайте каждый испытательный пакет перед обработкой.
Некоторые специалисты ошибочно начинают интегрирование F₀ только с начала фазы выдержки, не учитывая летальность, накопленную во время разогрева. Хотя летальность при разогреве (температуры ниже целевой) меньше, чем при выдержке, она реальна и должна учитываться. Профилактика: интегрируйте L от нулевого момента времени до конца охлаждения.
Воздух является теплоизолятором. Любой воздух, остающийся в реторт-устройстве во время обработки, создаёт зоны, в которые пар не проникает, что резко снижает местную теплопередачу. Схема вентилирования — последовательность и время открытия вентилей для вытеснения воздуха перед герметизацией устройства — должна быть валидирована в рамках HDS. Профилактика: включайте проверку схемы вентилирования в HDS явным образом.
Инкубационный тест должен проводиться при 35°C ± 1°C в течение ровно 10 дней с минимальным размером выборки 24 пакета на партию. Распространённые ошибки: использование инкубатора без проверки температуры, инкубация менее 10 дней, недостаточный размер выборки. При обнаружении вздутого пакета в процессе инкубации необходимо немедленно поместить в карантин 100% производственной партии. Профилактика: используйте откалиброванный инкубатор, ежедневно фиксируйте температуру, пересчитывайте единицы выборки перед началом.
Минимальное F₀ для коммерчески распространяемых низкокислотных пищевых продуктов в США составляет 3,0 минуты согласно 21 CFR Part 113. Это соответствует снижению спор C. botulinum на 12 log-единицы. На практике большинство коммерческих продуктов ориентировано на F₀ = 6–15 минут для обеспечения запаса безопасности при вариациях производственных условий. Ваш Process Authority устанавливает плановое F₀ для вашего конкретного продукта.
Да. Каждая рецептура, влияющая на теплопроникновение — плотность, вязкость, размер частиц, вес наполнения — требует собственного HPS. Плановый процесс, разработанный для куриного бульона, нельзя применять к более плотному рагу из курицы с овощами, даже в одной структуре пакета. Структура пакета (HDS, квалификация реторт-устройства) может использоваться совместно для нескольких продуктов; продукт-специфическое HPS — нет.
Полный срок валидации процесса составляет 14–22 недели. Два элемента с фиксированным временем: (1) минимум 3 запуска HPS — последовательные запуски могут быть выполнены за 1–2 недели, но меньшее число запусков неприемлемо; (2) 10-дневный инкубационный тест — это биологический тест, который невозможно сократить или ускорить никаким способом. Для рынка США время обработки регистрации в FDA (2–4 недели) добавляет дополнительный срок.
Да, при определённых условиях. Если ваш продукт будет обрабатываться в том же реторт-устройстве, что использовалось для HDS коупакера, в той же конфигурации загрузки, и данные HDS актуальны (как правило, не старше 3 лет и после значительных изменений оборудования), вы можете использовать их данные HDS для вашей валидации. Именно так работа с проверенным коупакером или поставщиком, как Sunkey — предоставляющим предварительно квалифицированные данные по устройству — может сократить временной план валидации. Обязательно согласуйте достаточность имеющихся данных HDS с вашим Process Authority.
Нарушение инкубации — наиболее серьёзный результат в процессе валидации. При обнаружении вздутого пакета немедленно: (1) поместите в карантин 100% производственной партии, связанной с этой инкубационной серией; (2) не распространяйте никакой продукт из этой партии; (3) немедленно уведомите Process Authority; (4) инициируйте полное расследование причин — данные термопар, рабочие записи реторта, данные о целостности швов партии; (5) для ранее распространённой продукции (если таковая имеется) — свяжитесь с FDA и начните оценку необходимости отзыва.
Структура пакета влияет на скорость теплопроникновения, а следовательно, на профиль накопления F₀ — но не меняет требование к F₀. Более тонкий пакет (например, 100 мкм суммарной толщины) нагревается быстрее и накапливает F₀ в холодной точке интенсивнее, чем более толстый пакет (например, 160 мкм). Однако плановый процесс должен быть валидирован для конкретной структуры пакета, используемой в производстве — переход на другую толщину или структуру требует повторной валидации HPS.
Большинство крупных импортирующих продовольственных рынков с формальными системами безопасности пищевых продуктов требует эквивалентной валидации процесса. Япония, Канада, Австралия/Новая Зеландия, Южная Корея и большинство стран ССЗ имеют нормативные требования к низкокислотным ретортным продуктам, функционально эквивалентные 21 CFR Part 113. Россия (стандарты ГОСТ Р, включая ГОСТ Р 51652 и серию ГОСТ Р ИСО) также требует документации о валидации процесса. Уточняйте требования для каждого целевого рынка у местного регуляторного консультанта.
Согласно 21 CFR Part 113, продукт не может быть законно продан в США до завершения регистрации планового процесса — даже если физически уже произведён. Произведённый до регистрации продукт должен оставаться на складе производителя или импортёра, помещённым в карантин, до момента подтверждения FDA регистрации. Планируйте производственный график с учётом 2–4-недельного срока обработки регистрации FDA. Отгрузка в США до завершения регистрации может привести к задержанию груза таможней или FDA при импортной проверке.
|
Получите данные предварительной квалификации — бесплатно Говорим по-русски. Sunkey предоставляет документированные данные исследования распределения тепла (HDS) и характеристики материалов для стандартных структур реторт-пакетов. Использование предварительно квалифицированных структур Sunkey позволяет сократить срок валидации, исключив HDS — вам потребуется только продукт-специфическое исследование теплопроникновения (HPS). Запросите пакет данных валидации без каких-либо обязательств: Email: bml@sunkeycn.com | WhatsApp: +86-138-1251-1247 www.sunkeypackaging.com | www.sunkeypackaging.ru ISO 9001 | ISO 22000 | BRC Packaging | FDA-registered | EU 10/2011 |